Zerwanie ścięgna Achillesa
Czy operacja jest zawsze konieczna?
Ścięgno Achillesa to największe ścięgno w ciele człowieka. W fachowej nomenklaturze nazywane jest również ścięgnem piętowym.
Achilles to nieustraszony wojownik z mitologii greckiej, posiadających jednak jeden słaby punkt – piętę! Jego matka Tetyda, pragnąc zapewnić mu nieśmiertelność, zanurzyła syna w wodach Styksu. Jedynym miejscem, które nie zostało zanurzone w wodzie była właśnie pięta, za którą go trzymała.
Kontuzje ścięgna Achillesa to jedne z najpopularniejszych problemów biegaczy1,2. Najczęściej problemy z Achillesem u biegaczy wynikają ze zbyt dużych przeciążeń i przyjmują postać zapalenia jego części ścięgnistej lub entezopatii przyczepu do kości piętowej. Kontuzje te potrafią naprawdę uprzykrzyć biegaczom życie. Zerwanie ścięgna Achillesa u biegaczy zdarza się znacznie rzadziej i jest częściej spotykane w sportach, które wymagają nagłych przyspieszeń np. piłka nożna, koszykówka czy siatkówka. Ostatnimi czasy obserwuje się wzrost częstości uszkodzeń – zerwania ścięgna Achillesa, ze względu na starzenie się społeczeństwa, rosnącą częstość występowania otyłości i zwiększone zaangażowanie w sport3.
Nie ma jednoznacznego konsensusu co do sposobu optymalnego leczenia zerwania ścięgna Achillesa. Ostatnie badania wykazały kluczową rolę rehabilitacji funkcjonalnej w leczeniu ostrych uszkodzeń ścięgna Achillesa, tym samym faworyzując leczenie zachowawcze.4
Stąd też leczenie zachowawcze (bezoperacyjne) zyskuje coraz większą popularność wśród ortopedów, gdyż pozwala uniknąć możliwego ryzyka wystąpienia powikłań pooperacyjnych. Nie mniej leczenie operacyjne jest nadal uważane za bardziej niezawodną opcję leczenia zerwania ścięgna Achillesa.
U kogo zrywa się ścięgno Achillesa?
Ze statystyk wynika, że mężczyźni są bardziej podatni na zerwanie ścięgna Achillesa niż kobiety5. Obserwowane są dwa wyraźne wzrosty występowania tej kontuzji. Pierwszy w grupie pacjentów pomiędzy 25 a 45 rokiem życia oraz drugi, u osób powyżej 60 roku życia6. Pierwszą grupę stanowią urazy wysokoenergetyczne, najczęściej związane z uprawianiem sportu. Drugą grupą są osoby starsze, u których uszkodzenie związane jest z niskoenergetycznym urazem zwyrodnieniowo zmienionego ścięgna.
Anatomia
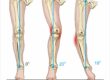
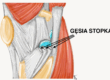
Ścięgno piętowe, bo tak brzmi anatomiczna nazwa ścięgna Achillesa. jest najsilniejszym i największym ścięgnem w ciele człowieka. Utworzone jest przez połączenie włókien ścięgnistych mięśnia brzuchatego łydki (łac. musculus gastrocnemius) i mięśnia płaszczkowatego ( łac.musculus soleus), które zlewają się w jedno ścięgno przyczepiając się do guza piętowego kości piętowej . Ścięgno Achillesa odgrywa kluczową rolę w przenoszeniu energii generowaną przez mięsnie tylnej grupy uda na podłoże, dzięki czemu możliwe jest odbicie stopy, To również bezpośrednie źródło jego dużego obciążenia. Ścięgno Achillesa mierzy średnio ok 15 cm. Część środkowa ścięgna, pomiędzy 2 a 6 cm powyżej guza piętowego, ma gorsze unaczynienie i to właśnie w tej strefie najczęściej dochodzi do uszkodzeń. Rysunek 1.

Rysunek 1. Ścięgno piętowe – ścięgno Achillesa największe ścięgno w ciele człowieka.
Elementy anatomiczne na rysunku:
1. mięsień brzuchaty łydki
2. mięsień płaszczkowaty
3. ścięgno Achillesa (ścienno piętowe)
4. guz piętowy
5 ścięgno podeszwowe
Rozpoznanie
Do rozpoznania zerwania ścięgna Achillesa wystarczy wywiad, to znaczy rozmowa z pacjentem i badanie ortopedyczne. Zazwyczaj badanie ortopedyczne nie pozostawia wątpliwości w diagnozie. W przypadkach wątpliwych można skorzystać z pomocy badania USG lub badania rezonansu magnetycznego. Typowy pacjent w wieku 30-40 lat podaje, że podczas biegu lub skoku poczuł nagły, ostry ból, który często porównuje do kopnięcia w łydkę. Niemożliwe staje się normalne chodzenie, bez utykania.
Zgodnie z wytycznymi Amerykańskiej Akademii Chirurgów Ortopedów, rozpoznanie ostrego zerwanie ścięgna Achillesa można postawić na podstawie występowania dwóch lub więcej z następujących objawów7:
- Test Thompsona: w pozycji leżącej na brzuchu, uciskamy pacjenta na łydkę. W przypadku zerwania ścięgna, test uznajemy za dodatni, gdy nie obserwujemy ruchu zgięcia podeszwowego stopy
- ubytek siły zgięcia podeszwowego stopy
- wyczuwalny palpacyjnie ubytek ścięgna zdjęcie 1
- zwiększone bierne zgięcie stopy
Zdjęcie 1. W badaniu wyczuwalny jest wyraźny ubytek ścięgna. Nie pozostawia to wątpliwości w diagnozie.
W przypadku całkowitego zerwania ścięgna, dla doświadczonego lekarza, rozpoznanie nie pozostawia wątpliwości i nie ma potrzeby wykonywania badań dodatkowych. Tym nie mniej, w przypadkach wątpliwych (uszkodzeniach częściowych, niekompletnych) diagnozę można potwierdzić badaniem usg lub badaniem rezonansu magnetycznego. Badanie rezonansu magnetycznego jest badaniem dokładniejszym (zdjęcie 2), aczkolwiek przewaga badania usg polega na możliwości wykonania badania dynamicznego. Podczas takiego badania można ocenić, czy kikuty ścięgna mają kontakt z sobą w momencie zgięcia podeszwowego stopy.
Ma to kluczowe znaczenie w przypadku kwalifikacji do leczenia nieoperacyjnego. Badanie klasyczne radiologiczne ma ograniczoną wartość i znajduje uzasadnienie w przypadku uszkodzeń zwyrodniałego ścięgna oraz uszkodzeń awulsyjnych guza piętowego.
Zdjęcie 2. Strzałka wskazuje uszkodzone ścięgno w obrazie rezonansu magnetycznego.
Leczenie zachowawcze – nieoperacyjne.
W Polsce dominuje pogląd o konieczności leczenia operacyjnego w przypadku ostrego zerwania ścięgna Achillesa. W krajach anglosaskich natomiast leczenie nieoperacyjne zyskuje coraz większą popularność i zastosowanie, aczkolwiek nadal nie ma konsensusu co do wyższości jednej metody nad drugą. Wiadomo, że operacja nie pozostawia wątpliwości co do zbliżenia końców ścięgna, natomiast wiąże się z ryzykiem powikłań infekcyjnych. Natomiast w przypadku leczenia nieoperacyjnego istnieje obawa dotycząca bezpośredniego kontaktu końców zerwanego ścięgna.
Leczenie zachowawcze polega na unieruchomieniu, założeniu opatrunku gipsowego, początkowo przez 4 tygodnie w zgięciu podeszwowym stopy (tak, aby maksymalnie zbliżyć końce ścięgna) a następnie, przez 2-4 tygodnie, w ustawieniu pośrednim stopy. Obserwacje wykazały, że leczenie nieoperacyjne niesie zwiększone ryzyko ponownego zerwania w porównaniu z leczeniem operacyjnym8. Ryzyko to można zminimalizować stosując we wczesnym etapie rehabilitację funkcjonalną, tym samym skracając okres unieruchomienia w gipsie9. W przeszłości uważano, że w przypadku leczenia nieoperacyjnego, rehabilitacja może być stosowana dopiero po zakończeniu okresu unieruchomienia w gipsie. Ten pogląd zweryfikowano, wprowadzając terapie funkcjonalna już po 3 tygodniach10,11.
W opracowanych protokołach rehabilitacyjnych stosuje się unieruchomienie przeciwdziałające nadmiernemu zgięciu grzbietowemu stopy (opatrunki gipsowe, ortezy), wymuszając pozycję stopy w zgięciu podeszwowym. Metoda rehabilitacji funkcjonalnej może być zastosowana w przypadku osób rozumiejących idee leczenia i współpracujących. Lepsze wyniki leczenia zachowawczego uzyskuje się w zerwaniach u osób młodych, u których nie doszło do zwyrodnieniowych zmian samego ścięgna.
Leczenie operacyjne
Możliwe są różne techniki zszycia końców ścięgna.
- Technika „open” – na otwarto, w której dostęp chirurgiczny pozwala na pełen wgląd do ścięgna.
- Technika „mini- open” w której wykorzystujemy małe nacięcia, aby przeprowadzić szwy.
- Technika szycia przezskórnego, najczęściej z wykorzystaniem podglądu usg 12.
Ograniczenie dostępu chirurgicznego służy ograniczeniu ryzyka powikłań infekcyjnych w leczeniu. Po operacji kończynę unieruchamia się w opatrunku gipsowym lub w ortezie.
Okres unieruchomienia po operacji jest dyskusyjny. Ostatnio podkreśla się rolę wczesnej rehabilitacji i wczesnego obciążania kończyny. Rehabilitacja musi być prowadzona na podstawie zwalidowanego protokołu rehabilitacyjnego, przez doświadczonego w tym zakresie fizjoterapeutę, unikając zgięcia grzbietowego stopy.
Powrót do zdrowia i sportu.
Średnio 12-18 tygodniu po operacji pacjenci są w stanie samodzielnie się poruszać zakładając, że zastosowano u nich właściwą rehabilitację. Rehabilitacja jest równie ważna jak sama operacja. Kryteria zaproponowane przez Van Sterkenburga i wsp, które muszą być spełnione, aby powrócić do biegania, zakładają umiejętność chodzenia na palcach, gdzie deficyt siły łydki kończyny operowanej musi być mniejszy niż ≤ 25% w porównaniu do strony zdrowej13. Powrót do sportów kontaktowych, w których dochodzi do nagłych przyspieszeń i hamowań, możliwy jest po odtworzeniu siły łydki, przy czym nie jest to proces szybki.
Podsumowanie
Zerwania ścięgna Achillesa zdarza się w 2 grupach chorych, młodszej u których do zerwania dochodzi w czasie aktywności sportowej oraz starszej, u której zerwanie spowodowane jest zamianami zwyrodnieniowymi ścięgna. W grupie młodszej można zastosować leczenie nieoperacyjne, przy czym jest ono bardziej wymagające, wymaga współpracy z pacjentem i doświadczonego fizjoterapeuty. W grupie starszej, z racji zwyrodnieniowych zmian ścięgna, zalecane jest leczenie operacyjne. W każdej z tych grup konieczne jest zastosowanie właściwej rehabilitacji, by móc wrócić do sprawności i sportu.
Bibliografia:
- Kakouris N, Yener N, Fong DTP. A systematic review of running-related musculoskeletal injuries in runners. J Sport Health Sci. Published online April 20, 2021. doi:10.1016/j.jshs.2021.04.001
- Lopes AD, Hespanhol LC, Yeung SS, Costa LOP. What are the Main Running-Related Musculoskeletal Injuries? Sports Medicine. 2012;42(10):891-905. doi:10.1007/bf03262301
- Raikin SM, Garras DN, Krapchev P V. Achilles tendon injuries in a United States population. Foot Ankle Int. 2013;34(4):475-480. doi:10.1177/1071100713477621
- Park SH, Lee HS, Young KW, Seo SG. Treatment of Acute Achilles Tendon Rupture. Clin Orthop Surg. 2020;12(1):1-8. doi:10.4055/CIOS.2020.12.1.1
- Movin T, Ryberg Å, McBride DJ, Maffulli N. Acute rupture of the Achilles tendon. Foot Ankle Clin. 2005;10(2):331-356. doi:10.1016/J.FCL.2005.01.003
- Möller A, Åström M, Westlin NE. Increasing incidence of Achilles tendon rupture. Acta Orthop Scand. 1996;67(5):479-481. doi:10.3109/17453679608996672
- Chiodo CP, Glazebrook M, Bluman EM, et al. Diagnosis and treatment of acute Achilles tendon rupture. J Am Acad Orthop Surg. 2010;18(8):503-510. doi:10.5435/00124635-201008000-00007
- Khan RJK, Fick D, Keogh A, Crawford J, Brammar T, Parker M. Treatment of acute achilles tendon ruptures. A meta-analysis of randomized, controlled trials. J Bone Joint Surg Am. 2005;87(10):2202-2210. doi:10.2106/JBJS.D.03049
- Willits K, Amendola A, Bryant D, et al. Operative versus nonoperative treatment of acute Achilles tendon ruptures: a multicenter randomized trial using accelerated functional rehabilitation. J Bone Joint Surg Am. 2010;92(17):2767-2775. doi:10.2106/JBJS.I.01401
- Saleh M, Marshall PD, Senior R, MacFarlane A. The Sheffield splint for controlled early mobilisation after rupture of the calcaneal tendon. A prospective, randomised comparison with plaster treatment. J Bone Joint Surg Br. 1992;74(2):206-209. doi:10.1302/0301-620X.74B2.1544953
- Hutchison AM, Topliss C, Beard D, Evans RM, Williams P. The treatment of a rupture of the Achilles tendon using a dedicated management programme. Bone Joint J. 2015;97-B(4):510-515. doi:10.1302/0301-620X.97B4.35314
- Hsu AR, Jones CP, Cohen BE, Davis WH, Ellington JK, Anderson RB. Clinical Outcomes and Complications of Percutaneous Achilles Repair System Versus Open Technique for Acute Achilles Tendon Ruptures. Foot Ankle Int. 2015;36(11):1279-1286. doi:10.1177/1071100715589632
- van Sterkenburg MN, Kerkhoffs GMMJ, van Dijk CN. Good outcome after stripping the plantaris tendon in patients with chronic mid-portion Achilles tendinopathy. Knee Surg Sports Traumatol Arthrosc. 2011;19(8):1362-1366. doi:10.1007/S00167-011-1514-0