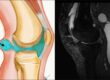
Przeciążeniowy ból piszczeli, czyli shin splints
Shin splints to najczęstsza kontuzja osób biegających.
Jaka jest jej przyczyna? Jak leczyć I zapobiegać tej kontuzji?
Badania naukowe potwierdzają moje obserwacje, że przeciążeniowy ból piszczeli (ang. MTSS medial tibial stress syndrome) to najczęstsza kontuzja biegaczy1,2 . Potocznie nazywany bywa również angielskim określeniem shin splints.
Ból obejmuje minimum 5 cm powierzchni przyśrodkowego brzegu piszczeli i wyraźnie wzmaga się podczas palpacji. Co charakterystyczne, bardziej nasilony bywa podczas początku aktywności z tendencją do ustępowania w trakcie wysiłku3. To częsty problem biegaczy, ale również może dotyczyć, piłkarzy, koszykarzy, tancerzy jak i personelu wojskowego (piechoty) z częstością występowania od 4 %do 35%4 . U biegaczy częstość występowania MTSS wynosi od 13% do 20%56. Uważa się, że przyczyną są nadmierne obciążenia, występujące w momencie uderzenia stopy o podłoże. Ból dotyka obszaru 1/3 dalszej kości piszczelowej o słabszym unaczynieniu i większej podatności. Część badaczy uważa, że może poprzedzać on zmęczeniowe uszkodzenie kości4. Przyczyną bólu jest zapalnie okostnej, któremu może towarzyszyć uszkodzenie warstwy korowej kości, aczkolwiek nie jest jasne, czy reakcja tkanek miękkich, czy uszkodzenie warstwy korowej kości występuje jako pierwsze. Etiologie kontuzji próbują wytłumaczyć teoria powiązania miejsca bólu z nadmierną pracą mięśni przyczepiających się w tym miejscu lub teoria bezpośredniego uszkodzenia kości. Ostatnio pojawił się doniesienia wiążące niedobór witaminy D3 mający wpływ na metabolizm kości i występowanie MTSS. W diagnostyce różnicowej zawsze należy brać pod uwagę złamanie zmęczeniowe kości. Badaniem, które różnicuje jest badanie rezonansu magnetycznego.
Jaka jest przyczyna bólu piszczeli?
Dokładna przyczyna MTSS nie jest w pełni poznana. Dominują dwie teorie: „teoria trakcji” i teoria oparta na modelu patologicznej adaptacji warstwy korowej kości piszczelowej na powtarzające działanie sił podczas biegu3,4.
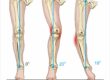
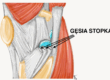
Zdjęcie 1.
Miejsce bólu w MTSS, obszar bólu na tylno-przyśrodkowym brzegu piszczeli ma więcej niż 5 cm.
| Czynniki ryzyka MTSS | |
| 1. | Płeć żeńska |
| 2. | BMI>21 |
| 3. | Nadmierna pronacja stopy-płaskostopie |
| 4. | Nadmiernie zniszczone biegowe buty |
| 5. | Ograniczenie zgięcia podeszwowego stopy |
| 6. | Nadmierna rotacja zewnętrzna biodra |
| 7. | Mała masa mięśniowa łydki |
| 8. | Początkujący biegacz |
| 9. | Historia wcześniejszych epizodów MTSS |
Tabela 1. Czynniki ryzyka MTSS na podstawie przeglądu systematycznego Karrie Hamstr-Wright i wsp22.
„Teoria trakcji” została po raz pierwszy zaprezentowana przez Devasa w 1958 roku, który stwierdził, że do zapalenia okostnej dochodzi w wyniku nadmiernej pracy (pociągania) mięśni łydki7.„Teoria trakcji” opiera się na połączeniu miejsca bólu z anatomicznym przyczepem włókien mięśniowych do tylno -przyśrodkowego brzegu kości piszczelowej.
W miejscu bólu na kości piszczelowej znajdują się przyczepy włókien mięśnia płaszczkowatego, zginacza długiego palców (FDL) i mięśnia piszczelowego tylnego (TP), co potwierdziły badania kadawerowe przeprowadzone przez Bouche i Johnsona8. Biorąc pod uwagę mechaniczne połączenie włókien Sharpeya, które są włóknami perforującymi, łączącymi okostną z kością, uważa się, że powtarzająca się praca mięśni może być podstawową przyczyną zapalenia okostnej. Jednak pozostaje niejasne, czy zapalenie okostnej występuje przed uszkodzeniem warstwy korowej kości piszczelowej, czy odwrotnie9.
Patologiczna adaptacja warstwy kości piszczelowej w wyniku powtarzających się naprężeń w momencie lądowania stopy w czasie biegu oraz pracy mięśni łydki, leży u podstawy drugiej teorii tłumaczącej MTSS 3,4. Największe siły koncentrują się na styku środkowej i 1/3 dalszej kości piszczelowej, gdzie trzon kości piszczelowej jest najwęższy. Zauważono, że u osób z MTSS pole przekroju kości piszczelowej oraz gęstość mineralne kości BMD (ang. bone mineral density) jest mniejsza niż w grupie kontrolnej 10,11. Zgodnie z prawem Delpecha-Wolffa siła wywierana na kość powoduje wyzwolenie komórkowej reakcji naprawczej mikrouszkodzeń i przebudowę kości 12.Niestety obciążenia powyżej pewnego zakresu wymykają się poza możliwość naprawy, kumulując się z czasem, prowadząc do uszkodzenia kości. Badania sugerują również, że słabsza siła mięśni łydki ma negatywny wpływ na proces adaptacji kości. MTSS rozwija się, gdy słabe mięśnie nie są w stanie przeciwstawić się siłom zginającym kość piszczelową, co skutkuje większym obciążeniem warstwy korowej kości piszczelowej10,13.
Wydaje się, że połączenie teorii trakcji okostnej przez mięśnie łydki i powtarzające się obciążenia zginające w poprzek kości piszczelowej są głównymi przyczynami MTSS. Warunki te oddziałują na siebie, tworząc patologiczne środowisko, którego organizm nie może zagoić. Reakcja zapalna okostnej jest dobrym wyjaśnieniem fazy ostrej, podczas gdy uszkodzenia kości mogą tłumaczyć fazę przewlekłą.
Czy MTSS poprzedza złamanie zmęczeniowe kości?
Można przyjąć założenie, że złamanie zmęczeniowe jest konsekwencją trwającego MTSS, co można tłumaczyć występowania złamań zmęczeniowych w tym samym miejscu tzn 1/3 dalszej kości piszczelowej. Jednakże złamania zmęczeniowe piszczeli obserwowane są również w innych miejscach piszczeli, co dowodzi, że jest to oddzielny mechanizm uszkodzeń14. Poza tym, zakładając, że ten sam uraz przeciążeniowy doprowadza do MTSS i złamań zmęczeniowych, to wszyscy pacjenci powinni doznać złamania zmęczeniowych po pewnym czasie, ale tak się nie dzieje. W obu przypadkach dochodzi do uszkodzenia warstwy korowej kości piszczelowej co jest spowodowane cyklicznym obciążaniem w momencie lądowania pięty na podłożu. Jednak geometria kości piszczelowej, jak i gęstość mineralna kości, różni się w obu przypadkach, co sugeruje inne biomechanizmy tych zjawisk10,15. Wymaga to jeszcze dalszych obserwacji i badań prospektywnych dla wyjaśnienia tych kwestii.
Niedobór witaminy D3?
Ostatnio pojawiła się praca Stürznickel i wsp., która dowodzi, że przyczyną nawrotowych obustronnych bólów piszczeli u biegaczy może być niedobór witaminy D 16,17. Niedobór witaminy D może prowadzić do powstania rzekomych złamań piszczeli, podobnych do tych obserwowanych w przypadkach osteomalacji. Co więcej, manifestacja złamań rzekomych nie jest konsekwencją zmienionej BMD ani mikroarchitektury, ale pojawia się u pacjentów ze wzrostem BMD wywołanym wysiłkiem fizycznym w połączeniu ze zmniejszonym poziomem 25-OH-D.
Postawienie właściwego rozpoznania.
Do postawienia rozpoznania MTSS upoważnia nas wywiad chorobowy pacjenta oraz dokładne badanie ortopedyczne.
Zazwyczaj pierwsze objawy bólu pojawiają się następnego dnia po intensywnym wysiłku. Ból zlokalizowany jest w 1/3 dalszej piszczeli, na jej tylno-przyśrodkowym brzegu na obszarze powyżej 5 cm 3,4,18,19. Zdjęcie 1.
Ból wyraźnie wzmaga się podczas dotyku (SEO) – podczas palpacji. Początkowo ból ma tendencje do ustępowania podczas trwania wysiłku. Niestety wraz z postępem choroby dolegliwości nasilają się do tego stopnia, że mogą występować w spoczynku i być przyczyną utykania. W diagnostyce różnicowej, w przypadku zespołu bólu piszczeli, należy zawsze brać pod uwagę złamanie zmęczeniowe oraz przewlekły zespół przedziałów powięziowych 18. W przewlekłym zespole przedziału wysiłkowego pacjenci zwykle opisują bolesny, związany z wysiłkiem fizycznym ucisk w przednio-bocznej części podudzia. Bólowi mogą temu towarzyszyć łagodne objawy neurologiczne. Ból nie pojawia się w spoczynku, ale nasila się podczas aktywności i szybko ustępuje po zaprzestaniu wysiłku fizycznego. W badaniu palpacyjnym nie stwierdza się typowej dla MTSS tkliwości20. Różnicowanie MTSS ze złamaniem zmęczeniowym jest trudniejsze. Ból jest zazwyczaj większy, bardziej zlokalizowany, ograniczony i punktowy, nie pozwala na treningi. W celu różnicowania rozpoznania istniej konieczność wykonania badania rezonansu magnetycznego21.
Czynniki ryzyka MTSS przedstawia tabela 1.
Badania dodatkowe
Zasadniczo rozpoznanie MTSS oparte jest na objawach klinicznych i u pacjentów z typową historią obciążeń treningowych i z typowymi objawami nie ma potrzeby wykonywania badań dodatkowych. W przypadku podejrzenia zmęczeniowego uszkodzenia kości tzn. gdy ból jest punktowy, na obszarze mniejszym niż 5 cm i wzmaga się podczas obciążeń, wówczas istnieje konieczność poszerzenia diagnostyki. Klasyczne zdjęcie radiologiczne ma ograniczoną wartość i służy raczej wykluczeniu innych przyczyn bólu4. Badanie rezonansu magnetycznego jest badaniem z wyboru i ma tę zaletę, że obrazuje zarówno obrzęk okostnej jak i szpiku kostnego, co pozwala rozróżnić ból piszczeli od zmęczeniowego uszkodzenia kości14,23. Fredericson i wsp. opracował w oparciu o wyniki badania rezonansu magnetycznego klasyfikacją rozróżniające MTSS od zmęczeniowego uszkodzenia kości wraz z przewidywanym czasem odpoczynku14.
| stopień | diagnoza | obraz mri | Zalecenia odpoczynku |
| 1 | MTSS | Łagodny do umiarkowanego obrzęk okostnej tylko na obrazach T2-zależnych; szpik: prawidłowy na obrazach T1- i T2-zależnych | minimum 3 tygodnie |
| 2 | MTSS | Obrzęk okostnej i obrzęk szpiku tylko na obrazach T2-zależnych | minimum 6 tygodni |
| 3 | Zmęczeniowe uszkodzenie kości piszczelowej | Obrzęk szpiku kostnego na obrazach T1- i T2-zależnych z obrzękiem okostnej lub bez niego | 12-16 tygodni |
| 4 | Zmęczeniowe uszkodzenie kości piszczelowej | Umiarkowany lub znaczny obrzęk okostnej i obrzęk szpiku zarówno na obrazach T1, jak i T2-zależnych; linia złamania wyraźnie widoczna na wszystkich sekwencjach | Powyżej 16 tygodni |
Tabela 2.
Klasyfikacja Fredricsona w oparciu o rezonans magnetyczny, rozróżniająca MTSS i zmęczeniowe uszkodzenie kości, z zalecanymi okresami odpoczynku14.
Leczenie
Leczenie polega na zaprzestaniu aktywności, które doprowadziły do kontuzji. W oparciu o klasyfikacje Fredricsona można oszacować czas potrzebnego odpoczynku. W przypadku gdy nie zostało wykonane badanie rezonansu, wówczas przerwa w treningu powinna trwać do całkowitego ustąpienia bólu, w tym również bolesności palpacyjnej piszczeli. W ostrej fazie bólu postępujemy zgodnie z protokołem RICE (rest, ice, compression, elevation), w tej fazie leczenia pomocne są krótkotrwale leki niesteroidowe przeciwzapalne, nie tylko łagodzące ból, ale skuteczne również poprzez efekt przeciwzapalny. Nie ma jednoznacznych dowodów co do skuteczności fizykoterapii w leczenie MTSS25. Jednakże wykazano, że terapia falą uderzeniową w połączeniu z odpowiednio dobranym treningiem biegowym skraca czas trwania objawów w porównaniu z samym treningiem26,27. Poza samym odpoczynkiem ważna jest profilaktyka kontuzji, to znaczy modyfikacja czynników ryzyka zależnych od pacjenta, przedstawionych w tabeli 1. Mam tu na myśli dobór wkładek ortopedycznych w przypadku nadmiernej pronacji stopy, rozciąganie i wzmacnianie mięśni łydki (mięśnia płaszczkowatego, mięśnia zginacza palucha i mięśnia piszczelowego tylnego), wzmacnianie stabilizacji miednicy i mięśni posturalnych28,29.
Pojawiają się opinie, że modyfikacja kroku biegowego może mieć wpływ na występowanie MTSS, predysponując zawodników biegających ze śródstopia30. W przypadku nawracających bólów piszczeli, szczególnie gdy problem występuje po obu stronach, należy oznaczyć stężenie witaminy D3 w surowicy, a w przypadku niedoboru rozpocząć suplementacje16,17. Istotna jest również edukacja pacjenta w zakresie właściwego planu treningowego, w którym znajduje się czas na nie tylko na trening biegowy, ale również stretching, ćwiczenia ogólnorozwojowe, regeneracje i odpoczynek. Niestety najczęstszym błędem jest postępowanie, które można opisać „za dużo, za szybko, za wcześnie”. Zbyt szybki wzrost objętości treningowych, bez właściwej regeneracji, u niedoświadczonych biegaczy kończy się kontuzją. Leczenie operacyjne jest bardzo rzadko wykonywane i nie ma naukowych dowodów potwierdzających skuteczność takiego leczenia3.
Kiedy możliwy jest powrót do treningu?
Powrót do aktywności sportowej można przewidywać na podstawie rezonansu magnetycznego i skali Fredricsona14. W praktyce, możemy posługiwać się dynamiką ustępowania dolegliwości bólowych, wówczas, gdy możliwe jest codzienne funkcjonowanie bez bólu oraz gdy ból nie występuje przy palpacji, można stopniowo powracać do treningu. W okresie rekonwalescencji możliwy jest trening na bieżni antygrawitacyjnej lub trening w wodzie, jeśli nie prowokuje on bólu. Trening na bieżni antygrawitacyjnej umożliwia dobór obciążenie pod kontrolą dolegliwości. W momencie powrotu do normalnych treningów, czas trwania biegu należy wydłużyć przed intensywnością, pamiętając, aby obciążenia zwiększać nie więcej niż 10% tygodniowo31.
Shin splints – Profilaktyka
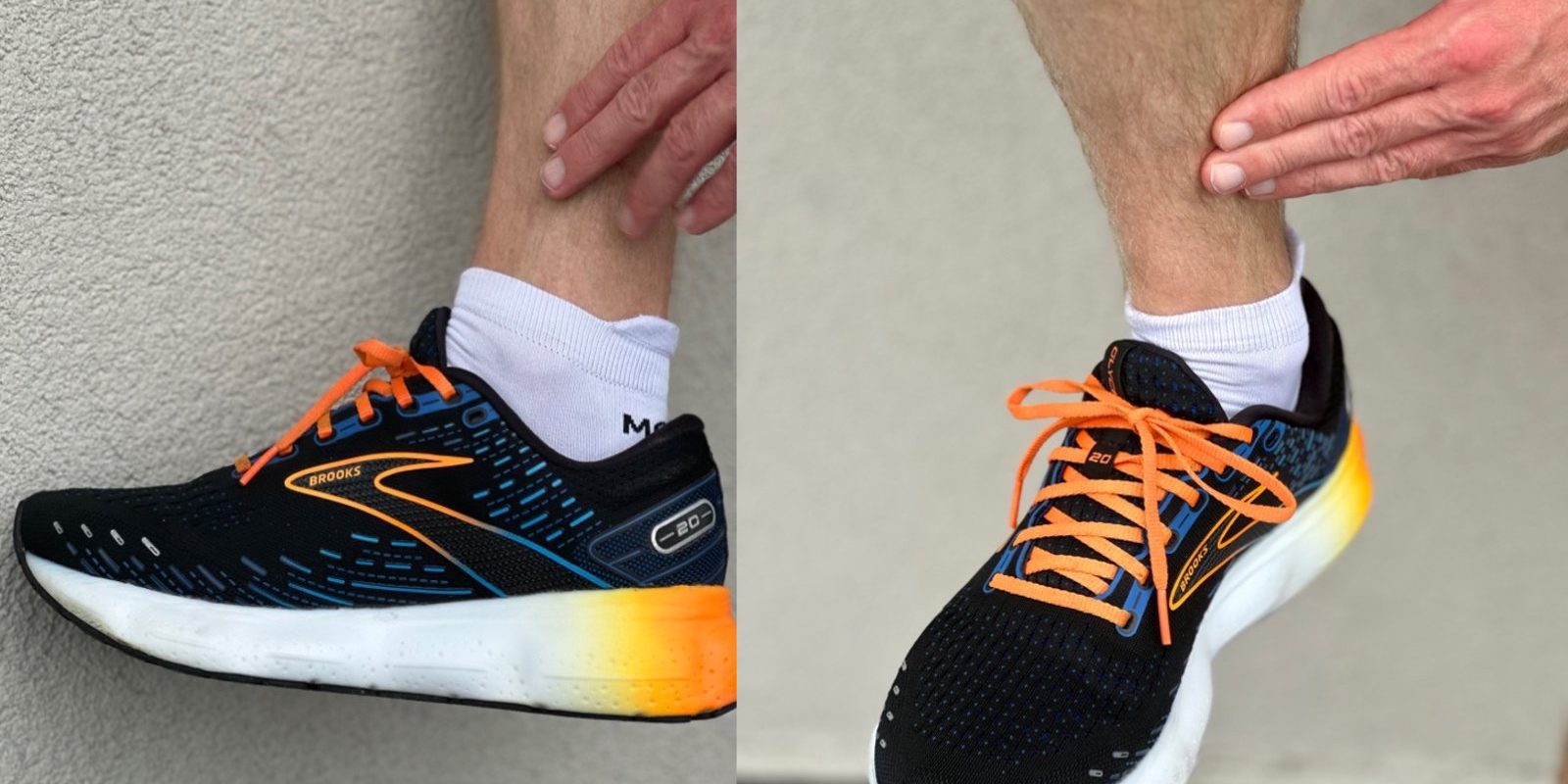
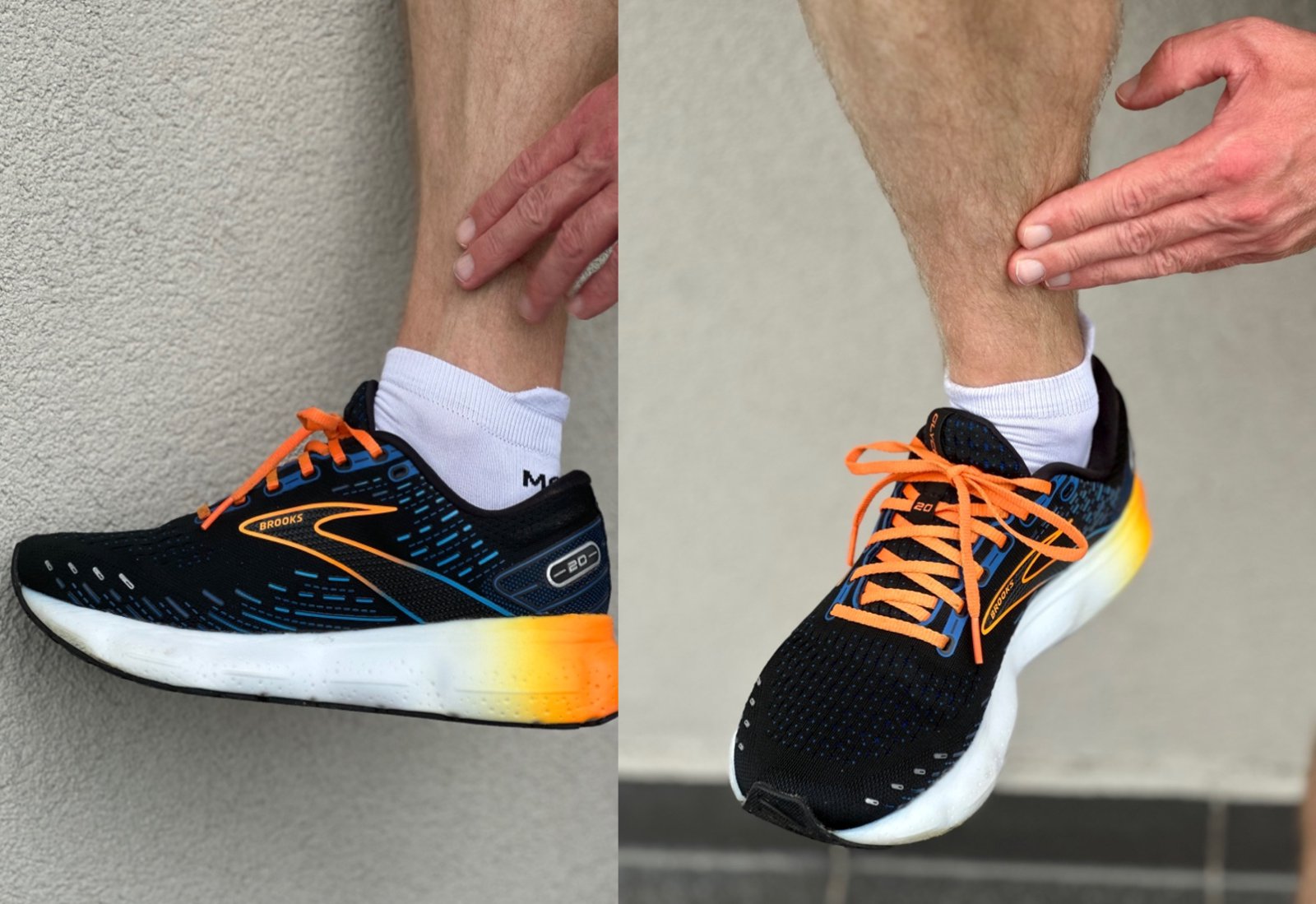
Każdego początkującego biegacza należy instruować, że trening biegowy nie polega tylko na samym bieganiu, ale również kształtowaniu ogólnej sprawności ze szczególnym uwzględnieniem mięśni stabilizujących miednicę, mięśni posturalnych i mięśni brzucha. Ustawienie miednicy w momencie podparcia ciała na jednej kończynę ma wpływ na obciążenia całej kończyny i ewentualne kontuzje. W profilaktyce MTSS znaczenie mają również właściwości amortyzacyjne butów biegowych. Ich amortyzacja zmienia się wraz z ilością przebiegniętych kilometrów i powinny być wymieniane po przebiegnięciu ok.500-1000 km32. Zdjęcie 2. W przypadku osób mających tendencje do nadmiernej pronacji stóp, istniej potrzeba doboru obuwia z przyśrodkową stabilizacją lub odpowiednich, dopasowanych wkładek ortopedycznych.
Shin splints aka ból piszczeli – Podsumowanie
Zespół bólowy piszczeli MTSS to częsta kontuzja biegaczy, która spowodowana jest nadmiernym przeciążeniem treningowym, powodującym zapalenie okostnej kości piszczelowej, a u niektórych osób może prowadzić do uszkodzenia warstwy korowej kości. Uważa się, że dwoma głównymi mechanizmami powstania kontuzji jest są zapalenie okostnej wywołane trakcją mięśni lub mikrourazami warstwy korowej kości. Pomimo licznych prac przeglądowych nadal nie ma konsensusu co do ostateczniej etiologii kontuzji: czy zapalnie okostnej jest pierwotne do uszkodzenia warstwy korowej, czy odwrotnie. Ostatnio pojawiła się koncepcja niedoboru witaminy D3 jako przyczyn nawracających i obustronnych epizodów bólu piszczeli. Do postawienia rozpoznania wystarczy dokładne zebranie wywiadu i badanie ortopedyczne. W diagnostyce różnicowej należy brać od uwagę przede wszystkim uszkodzenie zmęczeniowe kości, badaniem umożliwiającym przeprowadzić diagnostykę różnicową jest badanie rezonansu magnetycznego. Na podstawie rezonansu można również przewiedzieć szacowany czas leczenia.
Leczenie zachowawcze jest leczeniem z wyboru i w zdecydowanej większości kończy się sukcesem. Leczenie polega przede wszystkim przerwie w treningu i regeneracji. Powrót do sportu możliwy jest po całkowitym ustąpieniu objawów. Wracając do treningu istotnej jest, aby zmodyfikować (ograniczyć) czynniki ryzyka zależne od pacjenta (poprawa stabilizacji mięśniowej, wkładki ortopedyczne, zmiana butów biegowych, redukcja masy ciała).
U osób z nawracającym obustronnym zespołem MTSS konieczne jest oznaczenia stężenia witaminy D3 i ewentualne wyrównanie jej niedoboru.
Bibliografia:
- Kakouris N, Yener N, Fong DTP. A systematic review of running-related musculoskeletal injuries in runners. J Sport Health Sci. Published online April 20, 2021. doi:10.1016/j.jshs.2021.04.001
- Lopes AD, Hespanhol LC, Yeung SS, Costa LOP. What are the Main Running-Related Musculoskeletal Injuries? Sports Medicine. 2012;42(10):891-905. doi:10.1007/bf03262301
- Moen MH, Tol JL, Weir A, Steunebrink M, Winter TCD. Medial tibial stress syndrome: a critical review. Sports Med. 2009;39(7):523-546. doi:10.2165/00007256-200939070-00002
- Reshef N, Guelich DR. Medial tibial stress syndrome. Clin Sports Med. 2012;31(2):273-290. doi:10.1016/J.CSM.2011.09.008
- Lopes AD, Hespanhol LC, Yeung SS, Costa LOP. What are the Main Running-Related Musculoskeletal Injuries? Sports Medicine. 2012;42(10):891-905. doi:10.1007/bf03262301
- Bennett JE, Reinking MF, Pluemer B, Pentel A, Seaton M, Killian C. Factors contributing to the development of medial tibial stress syndrome in high school runners. J Orthop Sports Phys Ther. 2001;31(9):504-510. doi:10.2519/JOSPT.2001.31.9.504
- DEVAS MB. Stress fractures of the tibia in athletes or shin soreness. J Bone Joint Surg Br. 1958;40-B(2):227-239. doi:10.1302/0301-620X.40B2.227
- Bouché RT, Johnson CH. Medial tibial stress syndrome (tibial fasciitis): a proposed pathomechanical model involving fascial traction. J Am Podiatr Med Assoc. 2007;97(1):31-36. doi:10.7547/0970031
- Winters M, Burr DB, van der Hoeven H, Condon KW, Bellemans J, Moen MH. Microcrack-associated bone remodeling is rarely observed in biopsies from athletes with medial tibial stress syndrome. J Bone Miner Metab. 2019;37(3):496-502. doi:10.1007/S00774-018-0945-9
- Franklyn M, Oakes B. Aetiology and mechanisms of injury in medial tibial stress syndrome: Current and future developments. World J Orthop. 2015;6(8):577-589. doi:10.5312/WJO.V6.I8.577
- Magnusson HI, Westlin NE, Nyqvist F, Gärdsell P, Seeman E, Karlsson MK. Abnormally decreased regional bone density in athletes with medial tibial stress syndrome. Am J Sports Med. 2001;29(6):712-715. doi:10.1177/03635465010290060701
- Frost HM. Bone’s Mechanostat: A 2003 Update. Anatomical Record – Part A Discoveries in Molecular, Cellular, and Evolutionary Biology. 2003;275(2):1081-1101. doi:10.1002/ar.a.10119
- Milgrom C, Radeva-Petrova DR, Finestone A, et al. The effect of muscle fatigue on in vivo tibial strains. J Biomech. 2007;40(4):845-850. doi:10.1016/J.JBIOMECH.2006.03.006
- Fredericson M, Bergman AG, Hoffman KL, Dillingham MS. Tibial stress reaction in runners. Correlation of clinical symptoms and scintigraphy with a new magnetic resonance imaging grading system. Am J Sports Med. 1995;23(4):472-481. doi:10.1177/036354659502300418
- Franklyn M, Oakes B, Field B, Wells P, Morgan D. Section modulus is the optimum geometric predictor for stress fractures and medial tibial stress syndrome in both male and female athletes. Am J Sports Med. 2008;36(6):1179-1189. doi:10.1177/0363546508314408
- Stürznickel J, Jandl NM, Delsmann MM, et al. Bilateral Looser zones or pseudofractures in the anteromedial tibia as a component of medial tibial stress syndrome in athletes. Knee Surg Sports Traumatol Arthrosc. 2021;29(5):1644-1650. doi:10.1007/S00167-020-06290-0
- Ruohola JP, Laaksi I, Ylikomi T, et al. Association between serum 25(OH)D concentrations and bone stress fractures in Finnish young men. J Bone Miner Res. 2006;21(9):1483-1488. doi:10.1359/JBMR.060607
- KORTEBEIN PM, KAUFMAN KR, BASFORD JR, STUART MJ. Medial tibial stress syndrome. Med Sci Sports Exerc. 2000;32(3 Suppl):S27-S33. doi:10.1097/00005768-200003001-00005
- Yates B, White S. The incidence and risk factors in the development of medial tibial stress syndrome among naval recruits. Am J Sports Med. 2004;32(3):772-780. doi:10.1177/0095399703258776
- Edwards PH, Wright ML, Hartman JF. A practical approach for the differential diagnosis of chronic leg pain in the athlete. Am J Sports Med. 2005;33(8):1241-1249. doi:10.1177/0363546505278305
- Moran DS, Evans RK, Hadad E. Imaging of lower extremity stress fracture injuries. Sports Med. 2008;38(4):345-356. doi:10.2165/00007256-200838040-00005
- Hamstra-Wright KL, Bliven KCH, Bay C. Risk factors for medial tibial stress syndrome in physically active individuals such as runners and military personnel: A systematic review and meta-analysis. Br J Sports Med. 2015;49(6):362-369. doi:10.1136/bjsports-2014-093462
- Beck BR, Bergman AG, Miner M, et al. Tibial stress injury: relationship of radiographic, nuclear medicine bone scanning, MR imaging, and CT Severity grades to clinical severity and time to healing. Radiology. 2012;263(3):811-818. doi:10.1148/RADIOL.12102426
- Kress HG, Baltov A, Basiński A, et al. Acute pain: a multifaceted challenge – the role of nimesulide. Curr Med Res Opin. 2016;32(1):23-36. doi:10.1185/03007995.2015.1100986
- [Low-energy laser therapy in medial tibial stress syndrome] – PubMed. Accessed April 12, 2023. https://pubmed.ncbi.nlm.nih.gov/7801390/
- Reilly JM, Bluman E, Tenforde AS. Effect of Shockwave Treatment for Management of Upper and Lower Extremity Musculoskeletal Conditions: A Narrative Review. PM and R. 2018;10(12):1385-1403. doi:10.1016/J.PMRJ.2018.05.007
- Moen MH, Rayer S, Schipper M, et al. Shockwave treatment for medial tibial stress syndrome in athletes; a prospective controlled study. Br J Sports Med. 2012;46(4):253-257. doi:10.1136/BJSM.2010.081992
- Schwellnus MP, Jordaan G, Noakes TD. Prevention of common overuse injuries by the use of shock absorbing insoles. A prospective study. Am J Sports Med. 1990;18(6):636-641. doi:10.1177/036354659001800614
- Pope RP, Herbert RD, Kirwan JD, Graham BJ. A randomized trial of preexercise stretching for prevention of lower-limb injury. Med Sci Sports Exerc. 2000;32(2):271-277. doi:10.1097/00005768-200002000-00004
- Napier C, Cochrane CK, Taunton JE, Hunt MA. Gait modifications to change lower extremity gait biomechanics in runners: a systematic review. Br J Sports Med. 2015;49(21):1382-1388. doi:10.1136/BJSPORTS-2014-094393
- Rajasekaran S, Finnoff JT. Exertional Leg Pain. Phys Med Rehabil Clin N Am. 2016;27(1):91-119. doi:10.1016/J.PMR.2015.08.012
- Galbraith RM, Lavallee ME. Medial tibial stress syndrome: conservative treatment options. Curr Rev Musculoskelet Med. 2009;2(3):127-133. doi:10.1007/S12178-009-9055-6